הקדמה
ברזל הוא אחד היסודות החשובים בביולוגיה של גוף האדם בשל מעורבותו בתהליכים פיסיולוגיים חיוניים, ובראשם הובלת חמצן בדם כחלק ממולקולת ההמוגלובין. חסר בברזל הינו הסיבה הנפוצה ביותר לאנמיה כרונית וההתוויה היחידה למעשה לשימוש בתוספי ברזל (כטיפול מניעתי או טיפולי).
אצל אדם בריא, רמות הברזל בגוף בכל רגע נתון יחסית קבועות, מכיוון שקיים מנגנון מחזור יעיל באופן יחסי, שמאפשר שימוש חוזר בברזל שנמצא בכדוריות דם בסוף חייהן. לפיכך, ההשלמה הנדרשת מהמזון אינה גדולה ומספיקה עבור רוב האוכלוסיה שצורכת מזון מגוון שמכיל ברזל. עם זאת, ישנן תת-אוכלוסיות שזקוקות לכמויות גדולות יותר של ברזל לעומת האוכלוסיה הכללית, כגון ילדים בתהליכי גדילה, נשים בהיריון, אנשים עם בעיות ספיגה (חולי צליאק, מטופלים לאחר כריתת מעי, מטופלים עם זיהום של Helicobacter Pylori ועוד), או שמאבדות כמויות גדולות יחסית של ברזל, כגון נשים בגיל הפוריות שמאבדות ברזל בווסת. קבוצות אלו מהוות את אוכלוסיית היעד העיקרית לטיפול בתכשירי ברזל.
תכשירי ברזל ניתנים בשתי צורות: מתן תוך-ורידי או מתן פומי. מתן תוך-ורידי עוקף את תהליך הספיגה במערכת העיכול ולכן מאפשר להעלות את רמת הברזל בגוף יחסית מהר, אולם הוא כרוך באי-נוחות עבור המטופל (לעיתים יש צורך באשפוז), כאבים במקום ההזרקה ושאר תופעות לוואי הקשורות להזרקה תוך-ורידית. לעומת זאת, מתן פומי נוח יותר למטופל, אולם בשל שונות גבוהה בתהליך הספיגה של הברזל במערכת העיכול וגורמים חיצוניים שיכולים להשפיע עליו, לא תמיד צורת טיפול זו מצליחה להשיג את מטרותיה ולהעלות את רמת הברזל בגוף במידה מספקת.
תהליך ספיגת הברזל במערכת העיכול
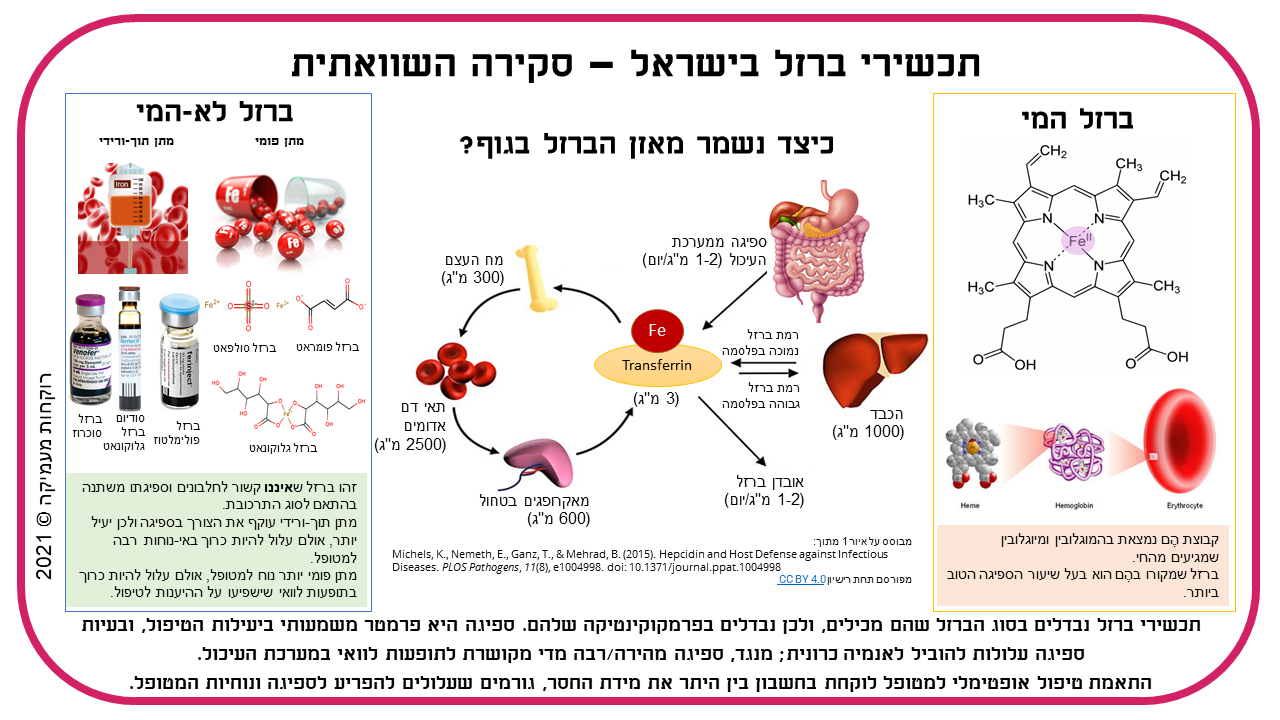
ברזל שמקורו במזון מתחלק לשני סוגים – ברזל המי (heme) וברזל לא-המי (non-heme):
ברזל המי נמצא בהמוגלובין ומיוגלובין שנמצאים בבשר, עופות ומאכלי ים. זוהי הצורה הקלה ביותר לספיגה בגוף מכיוון שמולקולות המוגלובין ומיוגלובין אינן מושפעות על ידי מרכיבי תזונה אחרים במזון, הן נספגות במסלול שונה מזה של הברזל הלא-המי והן אינן מושפעות משינויי ה-pH בין הקיבה לתריסריון כמו ברזל לא-המי (ר’ בהמשך).
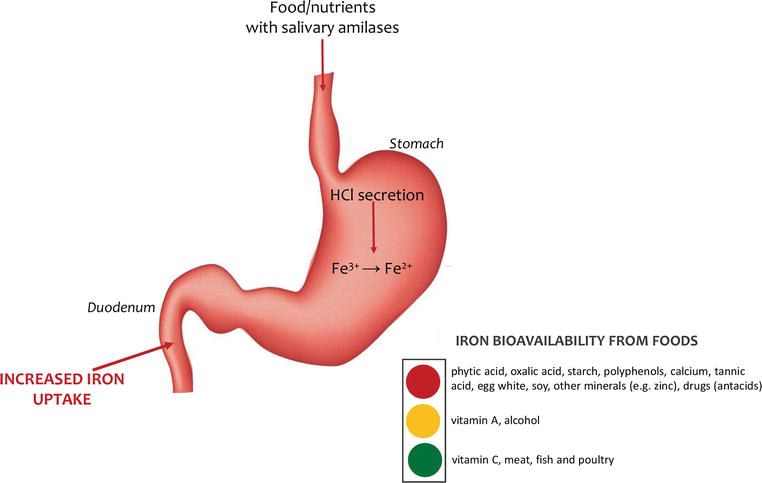
ברזל לא-המי הוא ברזל שאינו קשור לחלבונים אלא מופיע בצורת מלחי ברזל שונים. הוא קיים במזונות צמחיים ומזונות מועשרים בברזל, וספיגתו נמוכה יותר מזו של ברזל המי, בין היתר מכיוון שחלק מיוני הברזל במזון נחשפים לחמצן ומתחמצנים מצורת ה-Fe2+) ferrous) לצורת ה-Fe3+) ferric), שהינה בלתי-מסיסה ולכן לא יכולה להיספג במערכת העיכול. חלק מתהליך הספיגה של הברזל במערכת העיכול כולל חיזור של יוני ה-ferric ליוני ferrous על ידי האנזים duodenal cytochrome B בחלק העליון של התריסריון (הקרוב לקיבה).
עיקר הספיגה של ברזל במערכת העיכול מתרחשת בתריסריון ובחלק הראשון של הג’ג’ונום, וכאמור, תלויה במידה רבה במצבו הפיזיקלי של יון הברזל. ב-pH החומצי של הקיבה יוני הברזל נמצאים במצב חמצון של 2+, שהינו המצב המועדף לספיגה, אולם ב-pH פיזיולוגי, יוני הברזל יימצאו במצב חמצון גבוה יותר
(Fe3+, ferric) ולא יוכלו להיספג בתאי המעי – זו הסיבה לכך ששימוש בסותרי חומצה כגון מעכבי משאבות פרוטונים או חוסמי קולטן H2 מפחית את ספיגת הברזל במערכת העיכול.
לאחר מעבר המזון מהקיבה אל התריסריון, המזון ממשיך להיות חומצי עד לעליית ה-pH בתריסריון, ולכן הברזל נספג באיזור זה של מערכת העיכול. כאמור לעיל, יוני ברזל שבכל זאת מגיעים לתריסריון במצבם המחומצן (למשל בעקבות תגובה עם חמצן בקיבה) מתחזרים על ידי האנזים duodenal cytochrome B ליוני ferrous שיכולים להיספג אל האנטרוציטים ומשם לדם.
גורמים נוספים שמפחיתים ספיגת ברזל (לא-המי): רכיבים תזונתיים כגון פיטאטים, פוליפנולים ואף סידן (שיכול לעכב גם ספיגה של ברזל המי), חלבוני חלב וביצים וגם סויה, חומצה אוקסאלית שנמצאת בתרד, שעועית ואגוזים שונים, ועוד. מנגד, הגורם העיקרי שנחשב למשפר ספיגה של ברזל הוא ויטמין C, שמסוגל לחזר חלק מיוני ה-Fe3+) ferric) ליוני Fe2+) ferrous) ובכך להפוך אותם למסיסים. עם זאת, מספר מחקרים מהשנים האחרונות מראים שייתכן שההשפעה הזו איננה משמעותית כפי שנחשבה בעבר (ר’ למשל: Cook & Reddy, 2001; Li et al., 2020 ברשימת המקורות).
השוואה בין התכשירים הקיימים בישראל
להלן מצורפת טבלת השוואה בין תכשירי הברזל השונים אשר רשומים במאגר התרופות של משרד הבריאות (עדכנית לאוגוסט 2021):
ברזל במתן תוך-ורידי
ברזל שניתן במתן תוך-ורידי הוא בדרך כלל קומפלקס של ברזל עם מולקולות פחמימניות (סוכרוז, קרבוקסימלטוז, גלוקונאט), שמטרתן לייצב את הקומפלקס ולהגן עליו מפני ספיחה של יוני ברזל נוספים מהדם. לאחר ההזרקה, הקומפלקס נבלע על ידי המקרופאגים של המערכת הרטיקולואנדותליאלית בתהליך של אנדוציטוזה, ולאחר מכן מפורק על ידי ליזוזום. יון ה-Fe2+) ferrous) שמשתחרר מהקומפלקס נכנס למאגר הברזל הזמין במקרופאג או מועבר החוצה לדם. שם הוא מתחמצן ליון Fe3+) ferric), שנקשר לחלבון טרנספרין, שמוביל אותו מהדם אל אתרי המטרה של הברזל – מח העצם לצורך סינתזה של המוגלובין או הכבד לשם אחסון על ידי פריטין.
ניתן לסווג תכשירי ברזל המיועדים למתן תוך-ורידי בשני אופנים: לפי יציבות (קרי, שונות קינטית – כמה מהר הברזל יכול להשתחרר מהליגנדים הפחמימניים) ולפי חוזק (קרי, שונות תרמודינמית – כמה חזק הליגנדים קשורים לברזל, כלומר, כמה אנרגיה דרושה כדי לנתק ביניהם). תכשיר יכול להיחשב ליציב (robust) או בלתי-יציב (labile), וגם להיחשב לחלש (weak) או חזק (strong), או מצבי ביניים. תרומת הברזל של כל תכשיר עומדת ביחס הפוך למשקל המולקולרי שלו, כלומר, קומפלקסים גדולים יותר משחררים כמויות קטנות יותר של ברזל חופשי. לכן, תכשיר כמו Ferinject, שמכיל ferric carboxymaltose והינו בעל משקל מולקולרי גבוה (מעל 100 kDa) נחשב ליציב וחזק, ולכן משחרר ברזל באופן מבוקר ונסבל היטב מבחינה קלינית גם במינונים גבוהים.
לעומת זאת, תכשירים המכילים קומפלקסים של ברזל וסוכרוז (כגון Venofer, משקל מולקולרי: 43~ kDa) נחשבים יציבים-למחצה ובעלי חוזק בינוני, ולכן נוטים לשחרר כמויות גדולות יותר של ברזל חופשי. הסכנה בכך היא קישור רב יותר של ברזל לטרנספרין עד כדי רוויה, מה שעלול להותיר בפלסמה כמויות גדולות של ברזל שאינו קשור לטרנספרין (non-transferrin bound iron, NTBI). ברזל זה נכנס לתאים שונים בגוף באופן בלתי-מבוקר ועלול להוביל לעקה חמצונית על רקע יצירה של רדיקלים חופשיים. על כן, Venofer גם כן ניתן במתן תוך-ורידי, אולם המינון המקסימלי פר מנה נמוך יותר ומשך המתן ארוך יותר בהשוואה לתכשירים יציבים יותר כגון Ferinject.
תכשירי ברזל בעלי משקל מולקולרי עוד יותר נמוך, כגון Ferrlecit שמכיל sodium ferric gluconate (משקל מולקולרי: 37.5~ kDa), נחשבים עוד יותר חלשים ובלתי-יציבים, מכיוון שהם נוטים לשחרר כמויות גדולות אף יותר של ברזל חופשי, שמובילות לרוויה של טרנספרין ולעלייה ברמות NTBI. לכן, יש להשתמש בתכשירים אלו בזהירות והמינונים שלהם נמוכים יחסית לתכשירים האחרים שהוזכרו לעיל.
ברזל במתן פומי
בשל התכונות הפיזיקו-כימיות של מלחי ברזל, הם נספגים בין היתר באופן פסיבי באמצעות מעבר בין התאים (paracellular route), כך שחלק מיוני ה-(Fe2+) ferrous נספגים ישירות לדם:
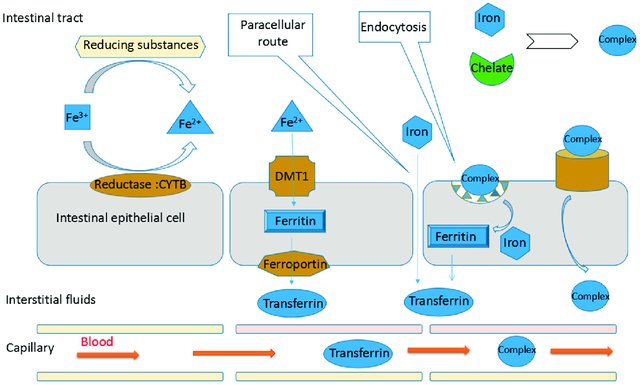
לכן, בעת נטילה של תכשיר ברזל שמכיל אחד ממלחי הברזל כגון ferrous citrate, ferrous sulfate, ferrous fumarate, רמת יוני הברזל בפלסמה עולה יחסית מהר, טרנספרין עלול להגיע לרוויה ויוני ברזל חופשיים נותרים בדם ועלולים להגיע למקומות בלתי-רצויים ולגרום לתופעות לוואי באופן תלוי-מינון (כלומר, מינון גבוה יותר גורם ליותר תופעות לוואי). לפיכך, דווקא תכשירים בעלי ספיגה מהירה אינם רצויים, ותכשירים המכילים Ferrous fumarate (כגון Forol, Folex, Foric pregnancy) עדיפים, מכיוון שזהו מלח הברזל בעל הנטייה הנמוכה ביותר לגרום תופעות לוואי, שכן קצב ההתמוססות שלו לאחר מתן פומי יחסית איטי, לעומת ferrous sulfate למשל, שמעלה את ריכוז הברזל בפלסמה (ואת ריכוז ה-NTBI) יחסית מהר, ולכן גורם לתופעות לוואי בשכיחות הגבוהה ביותר.
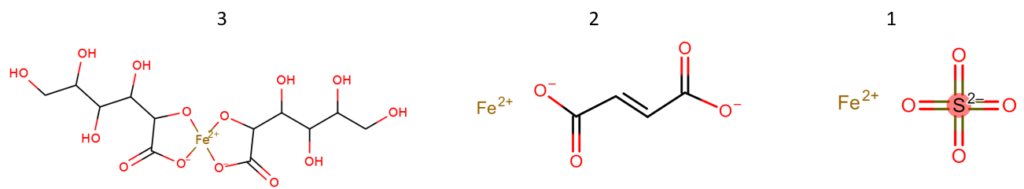
חשוב לזכור שמכיוון שתהליך ספיגת הברזל עלול להגיע לרוויה, עלייה במינון לא בהכרח תביא לעלייה פרופורציונלית בריכוז הברזל בפלסמה, כך שלא מדובר בפרמקוקינטיקה לינארית ולא ניתן להעריך את השפעת המינון על הרמות בפלסמה. במקרים שבהם מטופלים נוטלים מינון גבוה של ברזל פומי (או ברזל במתן תוך-ורידי בעל משקל מולקולרי יחסית נמוך) לאורך זמן במטרה לתקן אנמיה כרונית, הם עלולים במקביל לסבול מתופעות לוואי על רקע עקה חמצונית בתאים לאורך זמן.
בנוסף למלחי ברזל, קיימים תכשירי ברזל למתן פומי המכילים קומפלקסים של ברזל-פולימלטוז (כגון Ferrifol). אלו קומפלקסים יציבים, ומכיוון שהברזל שבהם אינו נמצא בצורתו היונית, הוא אינו מגיב עם חומרים במזון ואינו מעודד יצירה של רדיקלים חופשיים. בהיותו קומפלקס גדול, ספיגתו איטית יותר (מכיוון שהברזל אינו יכול לעבור בין התאים), אולם היא גוברת בנוכחות מזון (בניגוד למלחי הברזל), ופרופיל תופעות הלוואי של תכשירים אלו טוב יותר מזה של המלחים.
זמינות ביולוגית של ברזל
זמינות ביולוגית מוגדרת בפשטות כ-‘מידת הספיגה של חומר פעיל מתוך הפורמולציה ומידת זמינותו באתר המטרה’. בדרך כלל, זמינות ביולוגית של תרופות נקבעת על פי ריכוזי התרופה בפלסמה. עם זאת, מודל זה מתאים לתרופות שעבורן מתקיימת אינטראקציה של ליגנד/קולטן, כך שריכוז הליגנד בפלסמה משמש כסמן לריכוז הליגנד בסביבת הקולטן שלו, וכך להיקף האינטראקציה והפעילות הפרמקולוגית. עם זאת, אתר המטרה של ברזל הוא תא הדם האדום, ולא ניתן להסיק מריכוז הברזל בפלסמה כמה ברזל שימש ליצירת המוגלובין בתאי הדם האדומים. מכיוון שתהליך יצירת תאי דם אדומים (אריתרופוייזיס) נמשך
כ-3-4 שבועות, מידת ניצול הברזל מגיעה לשיאה רק לאחר 2-3 שבועות מהמתן, ומדידות של ריכוז הברזל בפלסמה בנקודות זמן קרובות לנטילת התכשיר אינן מעידות על יעילות הטיפול.
כמה מילים על תכשירי ברזל המסווגים כתוספי תזונה
תכשירי ברזל שמוגדרים כתוספי תזונה (קרי, אינם רשומים במאגר התרופות של משרד הבריאות ואינם מפוקחים על ידו) יכולים להכיל צורות שונות של ברזל ובמינונים שונים, ובהתאם לכך פוטנציאל היעילות שלהם משתנה:
Ferrous sulfate – קיימים בשוק תכשירים כגון Aktiferrin (שמכיל ferrous sulfate, לצד חומצת האמינו סרין ו/או חומצה פולית). מלח הסולפאט כבר נדון לעיל – מחד נספג במהירות, מאידך עלול לגרום לתופעות לוואי בשכיחות גבוהה על רקע הספיגה המהירה יחסית.
Ferrous gluconate – ישנם תוספי תזונה כגון תוסף הברזל של פלורדיקס, שמכילים את מלח הגלוקונאט של ברזל. גם מלח זה כבר נדון לעיל וספיגתו יחסית טובה מכיוון שגם הוא מכיל יוני Ferrous. עם זאת, תכולת הברזל נמוכה יחסית למשקל המולקולה (ר’ חישוב לדוגמא בסעיף הבא). המשמעות היא יחסית מעט ברזל בכל יחידת מתן – לדוגמא, על פי אתר החברה, בתוסף הברזל של פלורדיקס יש 3.75 מ”ג ברזל גלוקונאט בכל 5 מ”ל של התכשיר. מדובר בכמות ברזל אלמנטלי קטנה מאוד בכל כפית, מה שמצריך נטילה של כמות גדולה יחסית בכל פעם.
Ferrous bisglycinate – תכשירים כגון ‘ברזל עדין’ או Iron Max מכילים מולקולת ברזל בשם ברזל ביסגליצינאט. כל מולקולה כזו מורכבת מיון ברזל (Fe2+ ,ferrous) ושתי מולקולות של גליצין, כפי שמופיע באיור הבא:
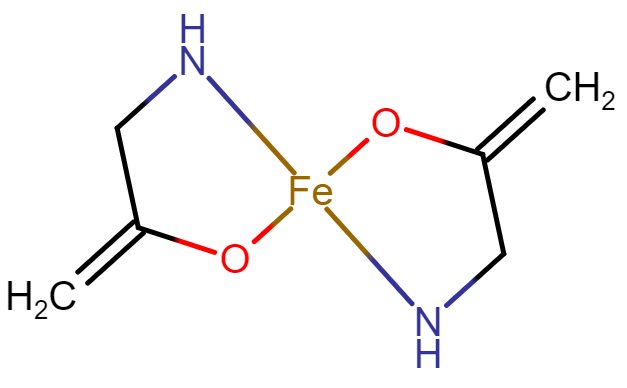
תרכובת ברזל זו הינה יחסית חדשה – בחיפוש ב-Pubmed המאמר הישן ביותר על ברזל זה פורסם בשנת 1999. אי לכך, כמות המחקרים אינה גדולה עדיין, ולמרות שהיצרנים מבטיחים ספיגה גבוהה יחסית למלחי ברזל, אין מספיק מחקרים שתומכים בכך.
Ferrous pyrophosphate – זהו מלח הברזל שנמצא בתכשיר ‘ברזל comfort’. מלח זה מכיל ברזל בצורת ה-Fe3+) ferric) ולכן בעל מסיסות נמוכה במים. עם זאת, ישנם מחקרים (למשל, Fidler et al., 2004) שמראים שברזל פירופוספאט שעבר מיקרוניזציה (גודל חלקיקים ממוצע: 0.3 מיקרון) יכול להתמוסס במים במידה טובה יותר ולכן ניתן להשתמש בו להעשרת מזונות נוזליים וספיגתו במערכת העיכול משתפרת – במחקר שלעיל היא נמצאה מקבילה לספיגה של ברזל סולפאט. כמו כן, קיימת כיום טכנולוגיה בשם Sucrosomial® Iron, אשר עוטפת את מלח הברזל בשכבה כפולה של פוספוליפידים ליצירת ליפוזומים, שגם כן אמורים לשפר את הספיגה. עם זאת, פורמולציות אלו עדיין יחסית חדשות ואין הרבה ספרות עליהן.
®Spatone – זהו תוסף תזונה נוזלי שמכיל מים עשירים בברזל, 5 מ”ג ברזל Fe2+) ferrous) בכל שקיק. תוסף זה מכוון לנשים בהיריון וישנם מחקרים שמראים שהוא יעיל יותר ונוח יותר לנטילה (עם פחות תופעות לוואי), אולם גם במקרה זה המחקרים מועטים מאוד (בסך הכל 6 תוצאות לחיפוש Spatone ב-Pubmed).
חישוב תכולת הברזל האלמנטלי בתכשיר ברזל
כיום רוב התכשירים מציינים באופן ישיר את כמות הברזל האלמנטלי ואת סוג המלח/התרכובת שנמצאים בתכשיר. עם זאת, כדאי להזכיר כיצד מחשבים את כמות הברזל האלמנטלי שנמצאת בתכשיר מסויים, אם נתונה כמות תרכובת הברזל וסוגה. כדי לחשב את כמות הברזל האלמנטלי בתכשיר, יש להתייחס למספר פרטים:
- כמות תרכובת הברזל ביחידת מינון (טבליה/5 מ”ל וכו’)
- המשקל המולקולרי של תרכובת הברזל
- המשקל המולקולרי של אטום הברזל (~55 מ”ג/מילימול)
בנוסף, חשוב לבדוק מהו היחס הסטויכיומטרי בין אטום הברזל לתרכובת עצמה – ברוב המקרים, כל מלח או תרכובת אורגנית של ברזל מכילים רק אטום ברזל אחד ולכן היחס הוא 1:1, מה שהופך את החישוב לפשוט יחסית. במקרים אחרים, יש לשים לב ליחס ולהתאים את החישוב כרשום להלן.
תהליך החישוב:
ראשית, יש לחשב כמה מילימולים של תרכובת ישנם ביחידה כמותית של תרכובת, באמצעות חלוקת הכמות (במ”ג) במשקל המולקולרי (במ”ג/מילימול). מתקבלת כמות המילימולים של התרכובת כולה, ואם היא מכילה רק אטום ברזל אחד, אזי זוהי גם כמות אטומי הברזל במילימולים באותה יחידת כמות (אם היחס אינו 1:1, יש להכפיל את כמות המילימולים ביחס יוני הברזל לתרכובת). את כמות הברזל במילימולים מכפילים במשקל המולקולרי של אטום ברזל (55.85) ומתקבלת כמות הברזל האלמנטלי במ”ג.
לדוגמא, ניתן לחשב את כמות הברזל האלמנטלי ב-5 מ”ל של תכשיר הברזל של פלורדיקס. על פי האתר, כל 5 מ”ל של סירופ מכילים 3.75 מ”ג של ברזל גלוקונאט (משקל מולקולרי: ~448 מ”ג/מילימול). לכן, מחלקים 3.75 מ”ג ב-448 מ”ג/מילימול ומתקבלים 0.0084 מילימולים של ברזל גלוקונאט. מכיוון שהמלח מכיל רק יון ברזל אחד בכל תרכובת, היחס הוא 1:1 ומספר המילימולים של המלח הוא גם מספר המילימולים של יוני הברזל. כעת מכפילים מספר זה במשקל המולקולרי של ברזל (55 מ”ג/מילימול) ומתקבל: 0.46 מ”ג של ברזל אלמנטלי בכל 5 מ”ל של הסירופ.
סיכום
ישנם תוספי ברזל מסוגים שונים ולכל אחד פרמקוקינטיקה שונה. הכרת ההבדלים בין התוספים מבחינת שיעור הספיגה הצפוי יכולה לסייע להתאים למטופל עם מאפיינים ייחודיים (היריון, מחלת צליאק וכו’) תוסף ברזל אופטימלי עבורו. פרמטרים נוספים שיכולים להשפיע על היעילות ועל ההיענות לטיפול מפורטים בטבלת ההשוואה המצורפת לפוסט, קרי, מתן תוך-ורידי או פומי, סיכון לתופעות לוואי במערכת העיכול, האם ניתן לרסק ועוד.
מקורות
Banjari, I. (2018). Iron Deficiency Anemia and Pregnancy. Current Topics In Anemia. doi: 10.5772/intechopen.69114
Cook, J., & Reddy, M. (2001). Effect of ascorbic acid intake on nonheme-iron absorption from a complete diet. The American Journal Of Clinical Nutrition, 73(1), 93-98. doi: 10.1093/ajcn/73.1.93
Ems T, St Lucia K, Huecker MR. Biochemistry, Iron Absorption. [Updated 2021 Apr 26]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2021 Jan-
Fernández-Bañares, F., Monzón, H., & Forné, M. (2009). A short review of malabsorption and anemia. World Journal Of Gastroenterology, 15(37), 4644. doi: 10.3748/wjg.15.4644
Fidler, M., Walczyk, T., Davidsson, L., Zeder, C., Sakaguchi, N., Juneja, L., & Hurrell, R. (2004). A micronised, dispersible ferric pyrophosphate with high relative bioavailability in man. British Journal Of Nutrition, 91(1), 107-112. doi: 10.1079/bjn20041018
Geisser, P., & Burckhardt, S. (2011). The Pharmacokinetics and Pharmacodynamics of Iron Preparations. Pharmaceutics, 3(1), 12-33. doi: 10.3390/pharmaceutics3010012
Gómez-Ramírez, S., Brilli, E., Tarantino, G., & Muñoz, M. (2018). Sucrosomial® Iron: A New Generation Iron for Improving Oral Supplementation. Pharmaceuticals, 11(4), 97. doi: 10.3390/ph11040097
Katzung, B. G., Masters, S. B., & Trevor, A. J. (2018). Basic & clinical pharmacology 14e, Chapter 33 – Agents Used in Cytopenias; Hematopoietic Growth Factors. New York: McGraw-Hill Medical
Kontoghiorghes, G., Kolnagou, A., Kontoghiorghe, C., Mourouzidis, L., Timoshnikov, V., & Polyakov, N. (2020). Trying to Solve the Puzzle of the Interaction of Ascorbic Acid and Iron: Redox, Chelation and Therapeutic Implications. Medicines, 7(8), 45. doi: 10.3390/medicines7080045
Lane, D., Bae, D., Merlot, A., Sahni, S., & Richardson, D. (2015). Duodenal Cytochrome b (DCYTB) in Iron Metabolism: An Update on Function and Regulation. Nutrients, 7(4), 2274-2296. doi: 10.3390/nu7042274
Li, N., Zhao, G., Wu, W., Zhang, M., Liu, W., Chen, Q., & Wang, X. (2020). The Efficacy and Safety of Vitamin C for Iron Supplementation in Adult Patients With Iron Deficiency Anemia. JAMA Network Open, 3(11), e2023644. doi: 10.1001/jamanetworkopen.2020.23644
Li, Y., Jiang, H., & Huang, G. (2017). Protein Hydrolysates as Promoters of Non-Haem Iron Absorption. Nutrients, 9(6), 609. doi: 10.3390/nu9060609
Martin‐Malo, A., Borchard, G., Flühmann, B., Mori, C., Silverberg, D., & Jankowska, E. (2019). Differences between intravenous iron products: focus on treatment of iron deficiency in chronic heart failure patients. ESC Heart Failure, 6(2), 241-253. doi: 10.1002/ehf2.12400
Pizarro, F., Olivares, M., Hertrampf, E., Mazariegos, D., & Arredondo, M. (2003). Research Communication: Heme-Iron Absorption Is Saturable by Heme-Iron Dose in Women. The Journal Of Nutrition, 133(7), 2214-2217. doi: 10.1093/jn/133.7.2214

דותן יקר,
אחת הסקירות הטובות והמקיפות ביותר שקראתי על תוספי הברזל ומי שמעוניין להבין טוב יותר על ההבדלים הקיימים והאפשרויות הטיפוליות – מומלץ לו לקרוא!
חסר תוסף ברזל שאני מוצאת אותו נוח למטופלים לנטילה ובעל הגיון פרמקולוגי בספיגה מוגברת-תכשיר ברזל על בסיס פורמולה ליפוזומלית, כגון Ecosupp.
אודה לך אם תוסיף נקודה זו לסקירתך המרשימה
הי ורדית, תודה על הערתך.
התייחסתי בקצרה לברזל ליפוזומלי בסעיף העוסק בברזל פירופוספאט. ישנם מספר תוספי תזונה בהם נעשה שימוש בפורמולציה ליפוזומלית להגברת הספיגה (ידוע לי גם על ויטמין C, ויטמין D3, כורכום ועוד), אבל לא מצאתי הרבה מחקרים איכותיים בבני אדם שאכן מעידים על שיפור בספיגה כתוצאה מהפורמולציה הליפוזומלית.
האם מניסיונך הפורמולציה אכן יעילה יותר מתוספי ברזל אחרים?
אני מכירה את שיטת המתן של פורמולציה ליפוזומלית מתכשירים אחרים אשר ניתנו למטופלים עם מורכבות טיפולית ובעיות ספיגה – כגון חולי CF. לחולי CF יש תכשירי מולטיויטמינים איכותיים אשר ניתנים כפורמולה ליפוזומלית והוכיחו הצלחה גם בשיפור מדדים בזרם הדם ובעיקר בשיפור תסמינים קליניים. ההצלחה של הספיגה היא לאו דווקא בגלל התוסף שנמצא בתוך הפורמולה, אלא בגלל הפורמולה הליפוזומלית שמשפרת את הספיגה כי היא “מחקה” את תהליכי הספיגה של מזון במערכת העיכול (לפחות ממה שזכור לי).
אולי שווה להכין פוסט על נושא הפורמולה הליפוזומלית או משפרי ספיגה למיניהם..??
לשאלתך, לעניין תכשירי ברזל ליפוזומליים באופן ספיציפי –
לא מכירה עבודות קליניות. לצערי, אני גם חושבת שלא יהיו כאלה בזמן הקרוב… כי זה יותר קשה כאשר המדובר בחברות קטנות דלות אמצעים של תוספי תזונה. וזאת להבנתי את המתרחש בשוק. מצד שני, כן מטפלת במטופלים שמוכנים לקחת את הפורמולות האלה, מתמידים כי הן פורמולות טעימות יותר, ואכן משתפרים להם המדדים בזרם הדם.
זה נכון שאותנו מלמדים לקבל החלטות לפי Evidence Based Medicine.
מצד שני, חשוב לזכור שלפני EBM יש את הבנאדם ויש את הטיפול.
טיפול תמיד היה ותמיד יהיה.
EBM הוא רק כלי.
כלי שמסייע בתהליך קבלת ההחלטות, אבל הוא לא מהות הטיפול.
בהצלחה!
סקירה גאונית וכתובה למופת.