
הקדמה
השמנת-יתר היא מצב רפואי בעל השלכות רבות על המטופל הבודד וגם על מערכת הבריאות כולה, מכיוון שלרוב נלווים אליה מצבים רפואיים נוספים כגון סוכרת מסוג 2, מחלות קרדיווסקולריות, כבד שומני לא-אלכוהולי, הפסקות נשימה בשינה, אוסטאוארתריטיס ועוד.
ארגון הבריאות העולמי (WHO) מגדיר עודף משקל (Overweight) במבוגרים כ-BMI ≥ 25 kg/m2 והשמנה (או השמנת-יתר, Obesity) כ-BMI ≥ 30 kg/m2. על אף הבעייתיות המובנית במדד ה-BMI (מבוסס על משקל גוף כולל שאינו מתייחס בהכרח לאחוז רקמות השומן בגוף), על פי ה-WHO זהו המדד השימושי ביותר ברמת האוכלוסיה מכיוון שהוא שימושי באותה מידה עבור גברים ונשים ובכל שכבות הגיל במבוגרים.
* לצורך נוחיות הכתיבה ייעשה בפוסט זה שימוש במונח ‘השמנת-יתר’ לתיאור כלל מצבי ההשמנה החורגים מהנורמה (BMI = 18.5-24.9 kg/m2).
הטיפול הראשוני והבסיסי ביותר בהשמנת-יתר הוא שינוי אורח חיים, הכולל מעבר לתזונה בריאה וביצוע פעילות גופנית סדירה. עם זאת, במקרים של קושי ביישום ו/או בהתמדה בשינוי אורח החיים, ניתן להוסיף טיפולים פרמקולוגיים על מנת לעודד את הירידה במשקל ובכך ליצור משוב חיובי שיקל על המטופל ליישם את המעבר לאורח חיים בריא.
על פי איגוד הגסטרואנטרולוגיה האמריקאי (American Gastroenterology Association, AGA), הטיפולים הפרמקולוגיים בהשמנת-יתר פותחו ואושרו עבור טיפול לטווח ארוך בהשמנת-יתר ויעילותם נחשבת גבוהה, אולם השימוש בהם עדיין מוגבל בפרקטיקה הקלינית השגרתית והשונות בין הרופאים בהתייחסות אליהם גבוהה, בין היתר עקב היכרות בלתי-מספקת עם הטיפולים השונים, גישה וזמינות מוגבלת והעדר כיסוי ביטוחי. בשל כך, פרסם האיגוד בחודש נובמבר 2022 הנחיות קליניות בנוגע להתערבויות פרמקולוגיות במטופלים מבוגרים הסובלים מהשמנת-יתר – AGA Clinical Practice Guideline on Pharmacological Interventions for Adults With Obesity.
פוסט זה יסקור את הנחיות ה-AGA ואת ההמלצות לטיפולים התרופתיים הכלולים בהן תוך ציון הטיפולים הזמינים בישראל, על מנת לספק מידע רלוונטי לאנשי מקצוע המטפלים במטופלים הסובלים מהשמנת-יתר וזקוקים לטיפול תרופתי לצורך סיוע בירידה במשקל ושיפור מצבם הבריאותי הכללי (הערה: בפוסט מובאים עיקרי ההנחיות, למידע נוסף מומלץ לעיין בהנחיות המלאות).
נקודות כלליות חשובות
- הנחיות ה-AGA אינן מיועדות לקבוע צורת טיפול אחידה, אלא להוות בסיס לקבלת החלטות מושכלות עבור מטפלים ומטופלים.
- ההמלצות המובאות בהנחיות הינן כלליות ויש לשקול את התאמתן לכל מטופל באופן פרטני.
- ההמלצות מתמקדות בתרופות לטיפול בהשמנת-יתר המאושרות על ידי ה-FDA ומיועדות לטיפול במבוגרים עם BMI ≥ 27 kg/m2 אשר אינם מגיבים באופן מספק לשינוי באורח החיים.
התרופות שעבורן נוסחו ההמלצות הן:
| שם גנרי | שם מסחרי | האם רשומה בישראל?* |
| semaglutide 2.4 mg | Wegovy | לא |
| liraglutide 3.0 mg | Saxenda | כן |
| phentermine-topiramate ER | Qsymia | לא |
| naltrexone-bupropion ER | Contrave | לא |
| orlistat | Xenical | כן |
| phentermine | Razin | כן |
| diethylpropion | Tenuate | לא |
| Gelesis100 oral superabsorbent hydrogel** | Plenity | לא (מוגדר ב-FDA כאמ”ר) |
** לא יידון במסגרת פוסט זה.
תקציר ההמלצות
ההמלצות מסוכמות בטבלה מספר 1 במסמך. על פי המלצה מספר 1, ה-AGA ממליץ להוסיף טיפולים תרופתיים למטופלים הסובלים מהשמנת-יתר לצד שינויים באורח החיים אם אלו אינם מסייעים לירידה הרצויה במשקל. כמו כן, הואיל והטיפול הוא כרוני, בחירת התרופה צריכה להיות מבוססת על הפרופיל הקליני של המטופל וצרכיו, כולל מצבים רפואיים נלווים, העדפת המטופל, עלויות וגישה לטיפול. חלק משיקולים אלו יקבלו התייחסות להלן בחלק העוסק בכל תרופה.
התרופות שה-AGA ממליץ להשתמש בהן הן:
- semaglutide 2.4 (המלצה מספר 2)
- liraglutide 3.0 (המלצה מספר 3)
- phentermine-topiramate ER (המלצה מספר 4)
- naltrexone-bupropion ER (המלצה מספר 5)
- phentermine (המלצה מספר 7)
- diethylpropion (המלצה מספר 8)
- Gelesis100 oral superabsorbent hydrogel (רק במסגרת מחקר קליני, המלצה מספר 9)
ה-AGA איננו ממליץ להשתמש ב:
- orlistat (המלצה מספר 6)
אנלוגים ל-GLP-1
semaglutide 2.4 mg
semaglutide 2.4 mg (Wegovy) היא תרופה יחסית חדשה מקבוצת האנלוגים ל-GLP-1, אשר אושרה על ידי ה-FDA לטיפול בהשמנת-יתר ביוני 2021.
סטטוס רישום בישראל: לא רשומה (התכשיר Ozempic אשר מכיל semaglutide במינונים אחרים רשום בישראל לטיפול בסוכרת מסוג 2 ולא לירידה במשקל)
מנגנון פעולה: semgalutide היא אנלוג ארוך-טווח לחלבון האנושי Glucagon-like peptide-1 (GLP–1), המתפקד כאגוניסט לקולטן ל-GLP-1. הקולטנים ל-GLP-1 נמצאים על גבי תאי בטא בלבלב, והפעלתם על ידי GLP-1 אנדוגני מפעילה שרשרת אירועים אשר בסופו של דבר מעודדים הפרשת אינסולין מהתאים, אשר מפחית את רמות הגלוקוז בדם. בנוסף, קולטני GLP-1 נמצאים במספר איזורים במוח המעורבים בוויסות התיאבון והפעלתם מובילה לדיכוי התיאבון.
הואיל ו-GLP-1 אנדוגני מפורק במהירות גבוהה יחסית על ידי אנזימים כגון dipeptidyl peptidase (DPP-4) ואחרים, לא ניתן להשתמש בו כתרופה ולכן פותחו אנלוגים בעלי מבנה דומה אך לא זהה ל-GLP-1 האנדוגני, על מנת לאפשר את פעילותו הביולוגית מצד אחד ולהאריך את שהותו בגוף מצד שני. ההומולוגיה (דמיון מבני) של Semaglutide ל-GLP-1 האנדוגני היא 94%.
בנוסף לעידוד שחרור אינסולין מהתאים והורדת רמות גלוקוז בדם, אנלוגים ל-GLP-1 מדכאים הפרשת גלוקגון וחלקם מעכבים את ריקון הקיבה (האנלוגים שנחשבים לבעלי פעילות קצרת-טווח – exenatide (Bydureon) בפורמולציה שניתנת פעמיים ביום ו-lixisenatide (Suliqua), איור 1).

עיקרי הראיות שהוצגו על ידי ה-AGA:
- 8 מחקרים אקראיים מבוקרים שנמשכו 52-72 שבועות, אשר בהם טופלו 2,658 אנשים ב-semaglutide לעומת 1,694 אנשים שטופלו בפלצבו, הראו ירידה ממוצעת של 10.76% במשקל הגוף תחת הטיפול ב-semaglutide. זהו שיעור הירידה במשקל הגבוה ביותר מבין התרופות שנבדקו לצורך כתיבת ההנחיות, ועל רקע זה ממליץ ה-AGA להעדיף את semaglutide 2.4 mg על פני תרופות אחרות לטיפול בהשמנת-יתר.
- semaglutide מפחיתה גם ערכי HbA1c (במקור התרופה אושרה לטיפול בסוכרת מסוג 2) ובעלת אפקט מגן על הלב, ולכן מומלץ לשקול אותה עבור מטופלים הסובלים מסוכרת ומחלות קרדיווסקולריות.
- תופעות לוואי נפוצות: תופעות לוואי במערכת העיכול (עצירות, כאבי בטן, שלשולים, בחילות והקאות). בנוסף, ידוע שאנלוגים ל-GLP-1 עלולים להעלות סיכון לדלקת הלבלב (פנקראטיטיס) ומחלות של כיס המרה.
- ככלל, הירידה במשקל תחת semaglutide היא המשמעותית ביותר מבין כל התרופות שנסקרו ופרופיל תופעות הלוואי הוא נסבל, אולם ה-AGA מדגיש כי קיימת שונות די גדולה בין המחקרים שנבדקו, וכי במטופלים עם סוכרת מסוג 2 שיעור הירידה במשקל עשוי להיות נמוך יותר מאשר במטופלים ללא סוכרת מסוג 2.
liraglutide 3.0 mg
liraglutide 3.0 mg (Saxenda) היא תרופה מקבוצת האנלוגים ל-GLP-1, אשר אושרה על ידי ה-FDA לטיפול בהשמנת-יתר במבוגרים בדצמבר 2014 ובילדים מגיל 12 ומעלה בדצמבר 2020. חשוב לציין ש-liraglutide אושרה במקור (בשנת 2010) לטיפול בסוכרת מסוג 2 במינונים אחרים ותחת שמות מסחריים שונים (ר’ להלן), ובעקבות תוצאות משביעות רצון במחקרים קליניים, קיבלה אישור נפרד לטיפול בהשמנת-יתר.
סטטוס רישום בישראל: רשומה (מלבד Saxenda רשומים בישראל שני תכשירים נוספים שמכילים liraglutide – התכשיר Victoza והתכשיר Xultophy, אשר מכיל בנוסף ל-liraglutide גם אינסולין degludec. יש לציין שגם Victoza וגם Saxenda מכילות את אותה כמות liraglutide במזרק – 18 מ”ג ב-3 מ”ל, אולם מדובר בתכשירים שונים עם מינונים שונים והתוויות שונות).
מנגנון פעולה: liraglutide היא אנלוג ל-GLP-1 בדומה ל-semaglutide (ההומולוגיה של liraglutide ל-GLP-1 האנדוגני היא 97%) ולכן היא פועלת באותו מנגנון של הפעלת הקולטנים ל-GLP-1, עידוד הפרשת אינסולין והפחתת רמות הסוכר בדם.
עיקרי הראיות שהוצגו על ידי ה-AGA:
- 8 מחקרים אקראיים מבוקרים שנמשכו לפחות 52 שבועות, אשר בהם טופלו 3,964 אנשים ב-liraglutide לעומת 2,498 אנשים שטופלו בפלצבו, הראו ירידה ממוצעת של 4.81% במשקל הגוף תחת הטיפול ב-liraglutide.
- כמו semaglutide, גם liraglutide מפחיתה ערכי HbA1c (במקור התרופה אושרה לטיפול בסוכרת מסוג 2) ובעלת אפקט מגן על הלב.
- תופעות לוואי נפוצות: תופעות לוואי במערכת העיכול (עצירות, כאבי בטן, שלשולים, בחילות והקאות. בנוסף, ידוע שאנלוגים ל-GLP-1 עלולים להעלות סיכון לדלקת הלבלב (פנקראטיטיס) ומחלות של כיס המרה.
שיקולים קליניים חשובים בטיפול באנלוגים ל-GLP-1
- על מנת להפחית את תופעות הלוואי במערכת העיכול, מומלץ להעלות את המינון של אנלוגים ל-GLP-1 בהדרגה בתחילת הטיפול, בהתאם להנחיות בעלוני התרופות.
- אין לשלב אנלוגים ל-GLP-1 עם מעכבי DPP-4 מכיוון שהאפקט הסינרגיסטי קטן מאוד ולא מצדיק את העלויות למטופלים ואת הסיכוי לעלייה בתופעות הלוואי. על אף ההיגיון הפרמקולוגי, השילוב אינו מומלץ על ידי האיגודים המקצועיים.
- אנלוגים ל-GLP-1 מעכבים את ריקון הקיבה ולכן עלולים להפריע לספיגה של תרופות אחרות שניתנות פומית במקביל לאנלוג ל-GLP-1.
- הסיכון להיפוגליקמיה עם אנלוגים ל-GLP-1 נמוך ביחס לתרופות אחרות לטיפול בסוכרת, מכיוון שאנלוגים ל-GLP-1 מעודדים שחרור אינסולין מתאי בטא בלבלב כתלות ברמת הגלוקוז בדם.
נגזרות אמפטאמינים עם או ללא חומרים נוספים
Phentermine עם או בלי Topiramate
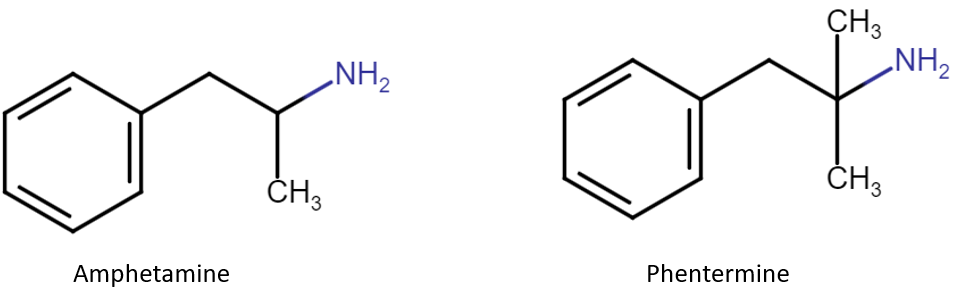
Phentermine (Razin) היא נגזרת של אמפטאמין (איור 2) שאושרה לראשונה על ידי ה-FDA בשנת 1959. Phentermine ו-Diethylpropion (ר’ בהמשך) אשר אושרה באותה שנה הן התרופות הוותיקות ביותר לירידה במשקל שעדיין נמצאות בשימוש קליני.
Topiramate (איור 3) היא תרופה ותיקה לטיפול בפרכוסים ובמיגרנות, אשר כלשעצמה איננה מאושרת כטיפול להורדת משקל, אולם משמשת למטרה זו במקרים מסויימים כשימוש שלא בהתוויה.
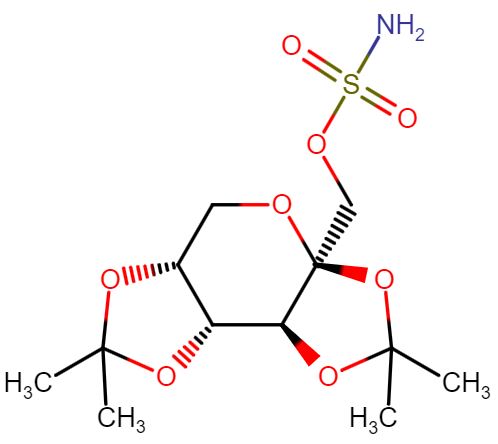
הערה: ניתן להבחין בחלק העליון של המולקולה בקבוצת סולפה (SO2NH2) אולם מכיוון שלא מדובר בתרופה אנטימיקרוביאלית (חסרת המבנה האופייני של אמין ארומטי), היא איננה צפויה לעורר תגובה אלרגית אצל אנשים הרגישים לתרופות סולפה (ר’ פירוט בפוסט “רגישות צולבת לתרופות סולפה“).
סטטוס רישום בישראל: Phentermine רשומה בישראל תחת השם המסחרי Razin. השילוב של Phentermine עם Topiramate (שם מסחרי: Qsymia) אושר על ידי ה-FDA ב-2012, אולם איננו רשום בישראל.
מנגנון פעולה: כאמור לעיל, Phentermine היא נגזרת של אמפטאמין ולכן יש לה תכונות סימפתומימטיות, ביניהן דיכוי תיאבון. כמו אמפטאמין ונגזרותיו, Phentermine מעכבת קליטה מחדש של נוראפינפרין ודופאמין ובכך מעלה את ריכוזו בסינפסה האדרנרגית והדופאמינרגית, בהתאמה (איור 4). העלייה ברמות נוראפינפרין ודופאמין מעודדת את פעילות המערכת הסימפתטית ותגובת Fight or flight, אשר בין היתר מדכאת תיאבון.
Topiramate היא תרופה אנטי-אפילפטית המשווקת משנת 1996 לטיפול בפרכוסים, ומשנת 2004 אושרה גם למניעת מיגרנות. מנגנון הפעולה שלה לירידה במשקל איננו ידוע. ישנה תיאוריה כי פעילותה של Topiramate כאנטגוניסט לקולטנים לגלוטמאט עשויה לתרום לירידה במשקל, אולם עדיין חסרות ראיות לכך.
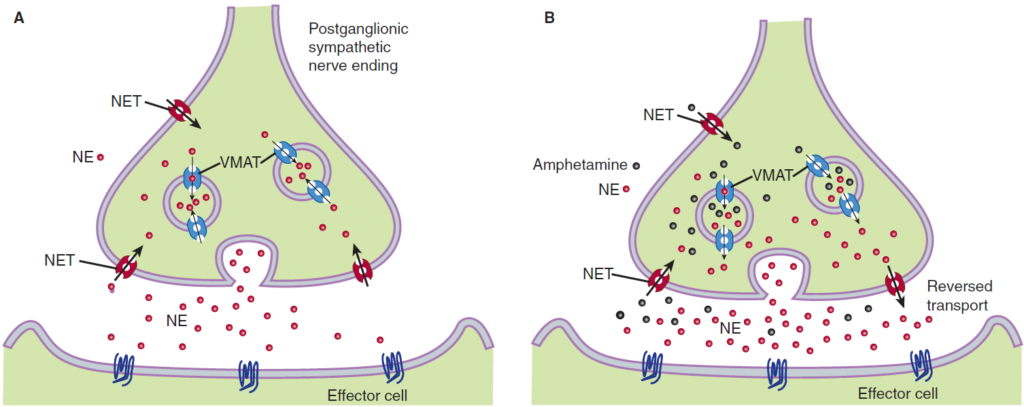
A: במצב רגיל, נוראפינפרין (NE) שמשתחרר מהעצב הפרה-סינפטי ומפעיל את הקולטנים בתא המטרה הפוסט-סינפטי נקלט מחדש בעצב הפרה-סינפטי דרך טרנספורטרים לנוראפינפרין (NET) שפרוסים על פני ממברנת קצה העצב. בתוך קצה העצב הפרה-סינפטי נוראפינפרין נכנס לווזיקולות שדרכן ישתחרר החוצה שוב תחת טריגר של פוטנציאל פעולה באמצעות טרנספורטר למונואמינים שנמצא על גבי הווזיקולה (VMAT).
B: תחת השפעת אמפטאמין מתרחשים שלושה שינויים בפעילות הסינפסה: חסימת קליטה מחדש של נוראפינפרין בתא הפרה-סינפטי, כניסה של אמפטאמין לווזיקולות דרך VMAT ודחיקה של נוראפינפרין החוצה, וכן עידוד הפרשה של נוראפינפרין דרך NET בתהליך שנקרא ‘טרנספורט הפוך’ (Reversed transport). כל ההשפעות האלו בסופו של דבר מעלות את ריכוז הנוראפינפרין בסינפסה וגורמות להפעלת יתר של הקולטנים בתאי המטרה ואפקטים סימפתומימטיים מוגברים.
עיקרי הראיות שהוצגו על ידי ה-AGA:
Phentermine-topiramate:
- 3 מחקרים אקראיים מבוקרים שבהם השתתפו בסך הכל 1,580 מטופלים בקבוצה שקיבלה phentermine-topiramate במינון של 15 מ”ג/92 מ”ג, לעומת 1,561 מטופלים בקבוצת הפלצבו, הראו ירידה ממוצעת של 8.45% במשקל הגוף הכולל.
- מינון של 7.5 מ”ג/46 מ”ג הוביל לירידה של 6.55% ממשקל הגוף הכולל.
- נצפתה ירידה קלה בלחץ הדם הסיסטולי והדיאסטולי תחת הטיפול בהשוואה לקבוצת הפלצבו.
- 17.4% מהמשתתפים בקבוצת phentermine-topiramate במינון של 15 מ”ג/92 מ”ג הפסיקו את הטיפול על רקע תופעות לוואי לעומת 8.5% בקבוצת הפלצבו.
- תופעות לוואי חמורות דווחו אצל 4.2% מהמשתתפים בקבוצת phentermine-topiramate במינון של 15 מ”ג/92 מ”ג לעומת 3.5% בקבוצת הפלצבו. תופעות לוואי נפוצות כוללות בעיות שינה (אינסומניה), פגיעה קוגניטיבית, עצירות, יובש בפה, נימול, שינויים בחוש הטעם ורגזנות.
Phentermine כמונותרפיה:
- 8 מחקרים אקראיים מבוקרים לטווח קצר (רובם ארכו 12 שבועות), ללא מחקרים שבחנו טיפול לטווח ארוך (מעל 52 שבועות). בקבוצת הטיפול נכללו בסך הכל 1274 מטופלים, ובקבוצת הפלצבו 730 מטופלים. במטה-אנליזה של התוצאות נצפתה ירידה ממוצעת של 3.63% ממשקל הגוף הכולל.
- 7 מתוך 8 המחקרים דיווחו על הפסקת טיפול על רקע תופעות לוואי וב-5 מחקרים דווח על תופעות לוואי חמורות. הסיבות העיקריות להפסקת הטיפול היו אינסומניה, רגזנות, חרדה, כאבי ראש, בחילות ועלייה בקצב הלב ובלחץ הדם.
שיקולים קליניים חשובים
- משך הטיפול המקסימלי ב-Phentermine המאושר על ידי ה-FDA ועל ידי משרד הבריאות הישראלי הוא 12 שבועות.
- Topiramate יעילה בטיפול בכאבי ראש מיגרנוטיים, ולכן יש להעדיף את השילוב של phentermine-topiramate במטופלים הסובלים ברקע גם ממיגרנות.
- יש להימנע מתכשירים המכילים Phentermine במטופלים עם היסטוריה של מחלה קרדיווסקולרית ויתר לחץ דם לא מאוזן, בשל הפעילות האדרנרגית של Phentermine והעדר מידע על בטיחות במטופלים עם רקע קרדיווסקולרי.
- Topiramate הוא טרטוגני, ולכן יש לוודא שימוש יעיל באמצעי מניעה בנשים בגיל הפוריות שמיועדות להשתמש בתכשיר.
- חשוב לנטר באופן עיתי את לחץ הדם וקצב הלב בעת נטילת תרופות המכילות Phentermine.
- למחקרי פאזה 3 גוייסו משתתפים עד גיל 70. אי לכך, אין מידע איכותי בנוגע לשימוש בתכשיר בקשישים.
- יש להימנע מתכשירים המכילים Phentermine גם במטופלים שמקבלים MAO inhibitors או שטופלו בהם ב-14 הימים האחרונים.
Naltrexone-bupropion ER
זהו תכשיר משולב המשווק תחת השם המסחרי Contrave, אשר מכיל Naltrexone ו-Bupropion בפורמולציה המיועדת לשחרור מושהה. התכשיר אושר על ידי ה-FDA בשנת 2014 כטיפול נלווה לצד שינוי באורח החיים עבור מבוגרים עם BMI ≥ 30 kg/m2 או BMI ≥ 27 kg/m2 עם לפחות סיבוך אחד שקשור להשמנת-יתר (יתר לחץ דם, סוכרת מסוג 2, דיסליפידמיה וכו’).
סטטוס רישום בישראל: לא רשום. בישראל אין כלל תכשירים רשומים המכילים Naltrexone, והתכשירים הרשומים שמכילים Bupropion הם Zyban ו-Wellbutrin, המיועדים להפסקת עישון ולטיפול בדיכאון, בהתאמה.
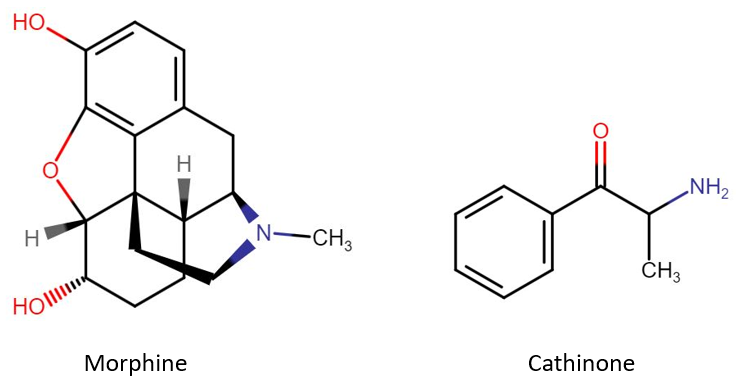
מנגנון פעולה: Naltrexone (איור 5) הוא אנטגוניסט אופיואידי, בהיותו נגזרת של מורפין (איור 6) עם שייר נפחי על אטום החנקן. בשל משך פעילות ארוך יחסית (מנה של 100 מ”ג חוסמת את ההשפעה של הירואין בהזרקה למשך 48 שעות), Naltrexone משמש כטיפול אחזקתי בהתמכרות לסמים, לעומת Naloxone, שהינו בעל משך פעילות קצר יותר ומשמש לטיפול אקוטי בהשפעות של מנת יתר באמצעות חסימת הקולטנים האופיואידיים (בעיקר קולטני μ). שימוש ב-Naltrexone מפחית את תחושת הכמיהה (craving) לסמים ואלכוהול ומקל על גמילה מניקוטין.
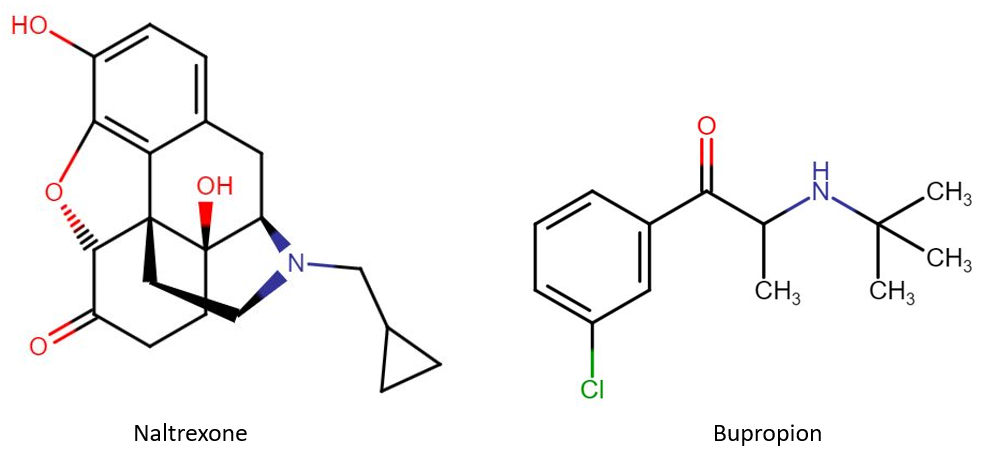
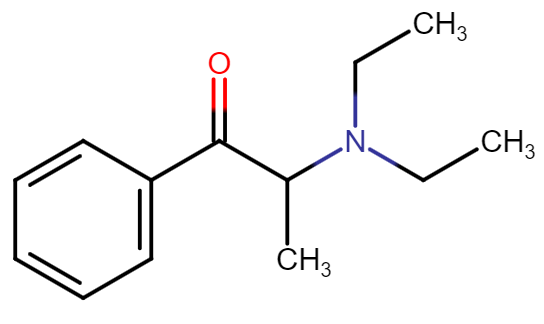
Bupropion (איור 5) הוא נגזרת של Cathinone (החומר הפעיל בצמח הגת, שהינו בעל מבנה דמוי-אמפטאמין, איור 6) והוא פועל באמצעות עיכוב קליטה מחדש של נוראפינפרין ודופאמין בסינפסה, וייתכן שאף גורם באופן ישיר לשחרור של קטכולאמינים.
המנגנון המדוייק שבו השילוב של Naltrexone ו-Bupropion מסייע להפחתה במשקל איננו ידוע.
עיקרי הראיות שהוצגו על ידי ה-AGA:
- נמצאו 5 מחקרים אקראיים מבוקרי-פלצבו לטווח ארוך (בסך הכל 6,947 משתתפים בקבוצות הטיפול ו-5,892 משתתפים בקבוצות הפלצבו; משך מעקב: 56 שבועות) אשר השוו את השילוב של Naltrexone-bupropion בשחרור מושהה לפלצבו ומצאו ירידה ממוצעת של 3% במשקל הגוף הכולל תחת הטיפול התרופתי לעומת פלצבו, עם סיכוי גבוה יותר להפחית 5%, 10% ו-15% ממשקל הגוף הכולל לעומת קבוצת הפלצבו.
- לא נמצא הבדל בין קבוצות הטיפול וקבוצות הפלצבו מבחינת חרדה ודיכאון כמצבים רפואיים נלווים או כתופעות לוואי לטיפול. לעומת זאת, במטופלים עם סוכרת מסוג 2 נמצאה ירידה קלה ב-HbA1C (ירידה של 0.6% בקבוצת הטיפול לעומת 0.1% בקבוצת הפלצבו).
- תופעות הלוואי הנפוצות תחת הטיפול התרופתי שגרמו להפסקת הטיפול היו בחילות, הקאות, כאבי ראש, סחרחורות ודיכאון, ללא הבדל משמעותי בתופעות לוואי חמורות בין הקבוצות.
שיקולים קליניים חשובים
- כדאי לשקול טיפול ב-Naltrexone-bupropion ER עבור מטופלים עם השמנת-יתר אשר מנסים להפסיק לעשן או סובלים מדיכאון, בשל ההשפעות המיטיבות שיש למרכיבים השונים של התכשיר על מצבים רפואיים אלו.
- לא מומלץ לתת תכשיר זה למטופלים הסובלים מיתר לחץ דם לא מאוזן, פרכוסים או כאלו שמשתמשים או השתמשו ב-14 הימים האחרונים במעכבי MAO. בנוסף, אין להשתמש בתכשיר זה בשילוב עם תכשירים אופיאטיים (סביב ניתוח או כטיפול כרוני).
- יש לנטר סימנים חיוניים במהלך הטיפול, בעיקר במהלך 12 השבועות הראשונים לטיפול. אין בשלב זה נתונים על תוצאים קרדיווסקולריים תחת הטיפול.
Diethylpropion
זוהי אחת התרופות הוותיקות לטיפול בהשמנת-יתר, אשר אושרה להתוויה זו על ידי ה-FDA בשנת 1959 (כמו Phentermine) במקביל לשינוי תזונתי ופעילות גופנית.
סטטוס רישום בישראל: לא רשומה
מנגנון פעולה: Diethylpropion (נקראת גם amfepramone) היא נגזרת של אמפטאמין (השוו למבנים של Bupropion ו-Phentermine) ולכן גם מנגנון הפעולה הוא אמפטאמיני (עיכוב קליטה מחדש של נוראפינפרין ודופאמין, אשר מדכאים תאבון – לפירוט ר’ הסעיף העוסק ב-Phentermine).
עיקרי הראיות שהוצגו על ידי ה-AGA:
- נמצאו 6 מחקרים אקראיים מבוקרי-פלצבו, שאורכם נע בין 52 שבועות ל-12 שבועות. יש לציין שאישור ה-FDA ניתן לטיפול קצר-טווח (עד 12 שבועות), על אף שמטופלים רבים ממשיכים את הטיפול למשך זמן ארוך יותר. רוב המחקרים כללו גם תזונה דלת-קלוריות, בדגש על תזונה דלת-שומן ופעילות גופנית.
- בכל ששת המחקרים דווח על ירידה במשקל, כאשר במטא-אנליזה של הנתונים נמצאה ירידה ממוצעת של 5.36% במשקל הגוף הכולל תחת Diethylpropion לעומת המטופלים שקיבלו פלצבו. בנוסף, למטופלים שקיבלו Diethylpropion היה סיכוי גבוה יותר לרדת 5% ומעלה ו-10% ומעלה במשקל הגוף הכולל מאשר בקבוצת הפלצבו.
- תופעות לוואי: לא נמצאו הבדלים משמעותיים בין הקבוצות, כולל שיעורי הפסקת הטיפול על רקע תופעות לוואי. הסיבות העיקריות להפסקת הטיפול היו אינסומניה, רגזנות או חרדה. באף אחד מהמחקרים לא דווחו תופעות לוואי חמורות.
- אף על פי כן, ה-AGA מעריך כי איכות העדויות נמוכה בשל חשד להטיות במחקרים, מרחב מדגם קטן יחסית והעדר נתונים לטווח ארוך.
שיקולים קליניים חשובים
- Diethylpropion קיימת בשתי פורמולציות: 25 מ”ג בשחרור מיידי לנטילה 3 פעמים ביום או 75 מ”ג בשחרור מושהה לנטילה פעם ביום בבוקר. בשני המקרים יש ליטול את התרופה לפני הארוחה.
- התרופה אינה מומלצת למטופלים עם היסטוריה של מחלה קרדיווסקולרית, ומומלץ לנטר אצל המטופלים לחץ דם וקצב לב באופן עיתי במהלך הטיפול.
- התרופה אינה מומלצת למטופלים הסובלים מהיפרתירואידיזם לא מטופל.
- תופעות לוואי נפוצות: עצירות, יובש בפה, אינסומניה, כאבי ראש ורגזנות.
מעכבי ליפאז
Orlistat
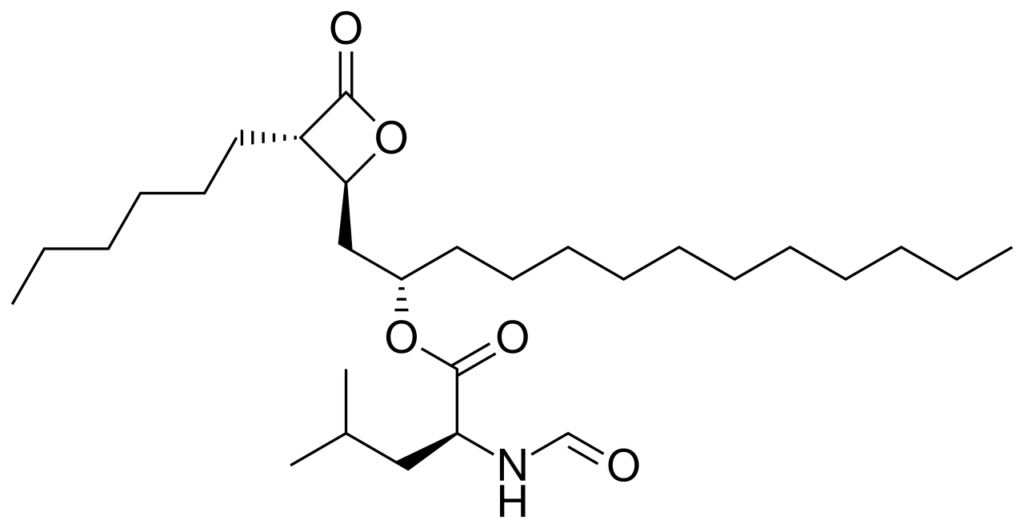
Orlistat (איור 7) אושרה על ידי ה-FDA לטיפול בהשמנת-יתר בשנת 1999 בשילוב עם תזונה דלת-קלוריות. בהנחיות העדכניות של ה-AGA, התרופה איננה מומלצת לשימוש כטיפול פרמקולוגי לירידה במשקל, שכן בשקלול הראיות (ר’ להלן) התועלת מהטיפול קטנה ביחס לנזק, מכיוון ששיעור הפסקת הטיפול גבוה משמעותית על רקע תופעות לוואי, שגם נחשבות טורדניות ביותר. עם זאת, ה-AGA מכיר בכך שעלות התרופה נמוכה ביחס לתכשירים חדשים יותר, ובכך שהתרופה איננה משפיעה על מערכת העצבים (בניגוד לתרופות שהוצגו לעיל – Topiramate, Phentermine, Naltrexone, Bupropion), כך שהפוטנציאל לתופעות לוואי נוירופסיכיאטריות נמוך, ולכן ייתכן שמטופלים מסויימים יעדיפו את Orlistat על פני אפשרויות טיפול אחרות. אי לכך, המלצת ה-AGA הינה מותנית ולא מוחלטת.
סטטוס רישום בישראל: רשומה בישראל תחת השם Xenical.
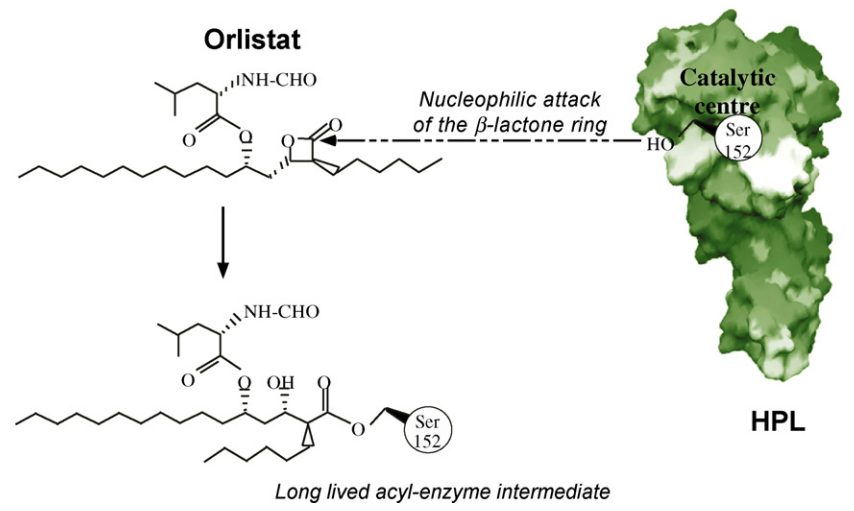
מנגנון פעולה: Orlistat היא מעכב של אנזימי ליפאז בחלל הקיבה והמעי הדק. התרופה נקשרת לאתר הפעיל של אנזימי ליפאז שמקורם בקיבה ובלבלב (איור 8) ובכך מונעת מהם לבצע הידרוליזה של כ-30% מהטריגליצרידים שמקורם במזון. באופן זה, השומנים אינם נספגים ואינם מספקים אנרגיה לגוף, מה שמוביל בסופו של דבר לירידה במשקל.
עיקרי הראיות שהוצגו על ידי ה-AGA:
- נמצאו 28 מחקרים אקראיים מבוקרי-פלצבו, שכללו 6,455 מטופלים שקיבלו Orlistat, לעומת 5,893 מטופלים שקיבלו פלצבו. אורך המחקרים נע בין 48 שבועות ל-4 שנים. רוב המחקרים כללו גם תזונה דלת-קלוריות, בדגש על תזונה דלת-שומן ופעילות גופנית.
- מתוך המחקרים הנ”ל, 15 מחקרים דיווחו על ירידה של 2.78% במשקל הגוף הכולל תחת Orlistat לעומת המטופלים שקיבלו פלצבו. בנוסף, למטופלים שקיבלו Orlistat היה סיכוי גבוה יותר לרדת 5% ומעלה ו-10% ומעלה במשקל הגוף הכולל מאשר בקבוצת הפלצבו.
- תופעות לוואי: לא נמצאו הבדלים משמעותיים בין הקבוצות, כאשר בקבוצה שקיבלה Orlistat שיעורי הפסקת הטיפול היו גבוהים יותר לעומת הפלצבו, על רקע תופעות לוואי במערכת העיכול: גזים, צואה שומנית, יציאות תכופות ועוד.
- קיימת אזהרה FDA בנוגע לפגיעה פוטנציאלית בכבד תחת טיפול ב-Orlistat, על רקע מספר דיווחים בארה”ב ומחוצה לה.
שיקולים קליניים חשובים
- למטופלים אשר נוטלים Orlistat מומלץ ליטול במקביל תכשיר מולטי-ויטמין המכיל ויטמינים מסיסי-שומן (A, D, E, K), במרווח של שעתיים לפחות מ-Orlistat.
- ישנן תרופות שספיגתן עלולה להיפגע במהלך הטיפול ב-Orlistat כגון Cyclosporine, Warfarin, Levothyroxine. אם לא ניתן להימנע מהשילוב, מומלץ לעקוב אחר רמות התרופות באופן הדוק יותר על מנת להימנע מפגיעה ביעילותן.
- הטיפול ב-Orlistat איננו מומלץ למטופלים עם בעיות ספיגה כרוניות, למשל על רקע שלשול כרוני, מחלת צליאק, מחלות מעי דלקתיות או ניתוח בריאטרי בעבר.
סיכום
השמנת-יתר היא מצב כרוני, אשר בעבר נחשב למחלה שניתנת לריפוי ולא למחלה כרונית, ולכן אין מידע לטווח ארוך על נגזרות האמפטאמינים שאושרו בסוף שנות ה-50 של המאה ה-20. עם זאת, תרופות חדשות לטיפול בהשמנת-יתר (כגון אנלוגים ל-GLP-1) כבר נדרשות להוכחת יעילות על פני טווח זמן ארוך יותר כחלק מההבנה שזהו הצורך הטיפולי.
מתוך שבע תרופות שנסקרו על ידי ה-AGA כאפשרויות טיפול בהשמנת-יתר, רק 3 רשומות בישראל – Saxenda (liraglutide), Razin (phentermine) ו-Xenical (orlistat), אשר על האחרונה ה-AGA איננו ממליץ לטיפול בהשמנת-יתר, בשל פרופיל תופעות לוואי אשר מקשה על היענות המטופל, ובפרט לטווח הזמן הנדרש, כפי שצויין לעיל.
מלבד מיעוט האפשרויות הזמינות בישראל, העניין הרב בתחום הטיפול הפרמקולוגי בהשמנת-יתר גורר שוק שלם של תכשירים “טבעיים” ותוספי תזונה שמבטיחים הרזייה מהירה וללא תופעות לוואי. המחלקה לפשיעה פרמצבטית במשרד הבריאות חשפה לא פעם כדורי הרזיה מזוייפים, אשר בבדיקת מעבדה התברר כי הם מכילים חומרים סימפתומימטיים מסוגים שונים – לרוב מדובר ב-Sibutramine, אשר דומה במבנהו לנגזרת אמפטאמין, אך פועל כמעכב קליטה מחדש של סרוטונין ונוראפינפרין (SNRI), ר’ למשל כאן וכאן. חומרים אלו, הנמצאים בכדורים בכמויות לא-ידועות, עלולים לגרום לנזקים חמורים כתוצאה משימוש בלתי-מבוקר.
לסיכום, הטיפול הפרמקולוגי בהשמנת-יתר הינו רק היבט אחד בטיפול הכולל במטופלים אלו. שינוי אורחות החיים (תזונה, פעילות גופנית) תמיד נמצא בבסיס הטיפול, ולצידו טיפול פרמקולוגי ותמיכה נפשית והתנהגותית, אשר מסייעים למטופל לראות תוצאות ולהתמיד באורח החיים החדש. בטיפול בהשמנת-יתר אין פתרונות קסם, והוא מבוסס על עבודה קשה והתמדה. ואם המטופל בכל זאת שואל על טיפולים טבעיים ו/או מהירים להרזייה, כדאי לומר לו ש:
If something sounds too good to be true, it probably is.
מקורות
Dailey, M. J., & Moran, T. H. (2013). Glucagon-like peptide 1 and appetite. Trends in Endocrinology & Metabolism, 24(2), 85–91. https://doi.org/10.1016/j.tem.2012.11.008
Grunvald, E., Shah, R., Hernaez, R., Chandar, A. K., Pickett-Blakely, O., Teigen, L. M., Harindhanavudhi, T., Sultan, S., Singh, S., Davitkov, P., & AGA Clinical Guidelines Committee (2022). AGA Clinical Practice Guideline on Pharmacological Interventions for Adults With Obesity. Gastroenterology, 163(5), 1198–1225. https://doi.org/10.1053/j.gastro.2022.08.045
Katzung, B.G. (2018) Basic & Clinical Pharmacology. 14th edn. New York: McGraw-Hill.
Lajthia, E., Bucheit, J. D., Nadpara, P. A., Dixon, D. L., Caldas, L. M., Murchie, M., & Sisson, E. M. (2019). Combination therapy with once-weekly glucagon like peptide-1 receptor agonists and dipeptidyl peptidase-4 inhibitors in type 2 diabetes: A case series. Pharmacy Practice, 17(4), 1588. https://doi.org/10.18549/pharmpract.2019.4.1588
Madsbad, S. (2015). Review of head-to-head comparisons of glucagon-like peptide-1 receptor agonists. Diabetes, Obesity and Metabolism, 18(4), 317–332. https://doi.org/10.1111/dom.12596
Meloni, A. R., DeYoung, M. B., Lowe, C., & Parkes, D. G. (2013). GLP-1 receptor activated insulin secretion from pancreatic β-cells: mechanism and glucose dependence. Diabetes, obesity & metabolism, 15(1), 15–27. https://doi.org/10.1111/j.1463-1326.2012.01663.x
Rubino, D.M. and Gadde, K.M. (2012) “A review of Topiramate and phentermine: A combined therapeutic approach for obesity,” Clinical Lipidology, 7(1), pp. 13–25. Available at: https://doi.org/10.2217/clp.11.65.
Tiss, A. et al. (2009) “Inhibition of human pancreatic lipase by tetrahydrolipstatin: Further kinetic studies showing its reversibility,” Journal of Molecular Catalysis B: Enzymatic, 58(1-4), pp. 41–47. Available at: https://doi.org/10.1016/j.molcatb.2008.11.003.
World Health Organization. (2021, June 9). Obesity and overweight. World Health Organization. Retrieved November 27, 2022, from https://www.who.int/news-room/fact-sheets/detail/obesity-and-overweight

כרגיל, מקצועי ומעניין
מקסים, כל הכבוד דותן!